有比获诺奖更重要的事情在等着我们一起去努力:救命!
今年,于瑞典当地时间10月1日,11:30AM(北京时间10月1日,17:30PM),诺贝尔评选委员会揭晓了今年的诺贝尔生理或医学奖获得者,James Allison和Tasuku Honjo,以表彰他们在癌症治疗:解除免疫抑制方面的的贡献。
 (图片来自诺奖官网)
(图片来自诺奖官网)
CTLA-4是是T细胞激活的抑制分子,在一些免疫疗法的尝试中(如癌症疫苗),T细胞上的CTLA-4的激活导致T细胞的活力被抑制(T细胞活性被踩了“刹车”),如果在治疗中,移除T细胞的“刹车”CTLA-4,那么T细胞就能重新对癌细胞发起攻击。James Allison的主要贡献在于明确了CTLA-4在肿瘤治疗中的价值,通过动物实验,他证明了CTLA-4的确有一定的抗癌作用,CTLA-4抗体可以增强免疫病治疗动物肿瘤。Tasuku Honjo的实验室则是PD-1的发现者,并认为它能参与细胞程序性死亡。1999年,他们敲除小鼠PD-1后,发现小鼠可发生自身免疫性疾病,提出PD-1有免疫抑制功能。
正如诺奖委员会所言,肿瘤免疫的重要性,在于它是一种新方法,传统的治疗仅是针对肿瘤,而这个方法针对免疫系统,并且该疗法适用于多种类型的肿瘤。但是,如果从目前的肿瘤免疫疗法回看,我们会发现两位的工作虽然有突破性意义,但是其中缺少了重要的一环。
CTLA-4对T细胞的作用是系统性的,系统性地激活T细胞会将免疫反应强制性地升高,甚至超出可以耐受的水平,这也是许多临床试验中,使用CTLA-4抗体治疗后,不良反应频率高的原因。而Honjo在发现了PD-1后,并没有将其与癌症治疗联系起来。事实上,也在1999年,梅奥诊所的陈列平教授从人正常细胞和肿瘤细胞中克隆并鉴定了一个名为B7-H1的分子,并证明该分子与T细胞的一个未知受体结合后,介导了免疫抑制。2000年,Honjo发现了PD-1的配体,PD-L1,该分子其实就是B7-H1,自此,PD-1/PD-L1通路介导肿瘤局部免疫抑制反应的理论才被打通。

后来数年间,陈列平教授证明PD-L1蛋白在多种肿瘤细胞中均有表达,肿瘤细胞上PD-L1的表达会促进T细胞的凋亡,使肿瘤的局部环境中,处于一个免疫抑制的状态。后续,陈列平团队使用单克隆抗体阻断PD-1/PD-L1的结合,通过解除局部免疫抑制,回复T细胞对肿瘤的杀伤作用。这种靶向局部免疫抑制,而不是系统性激活的方法,在治疗的同时,降低了治疗的副作用。这才是现在Opdivo,Keytruda等一系列如雷贯耳的肿瘤免疫药物的开端。此后,这些肿瘤免疫药物挽救了无数患者的生命。
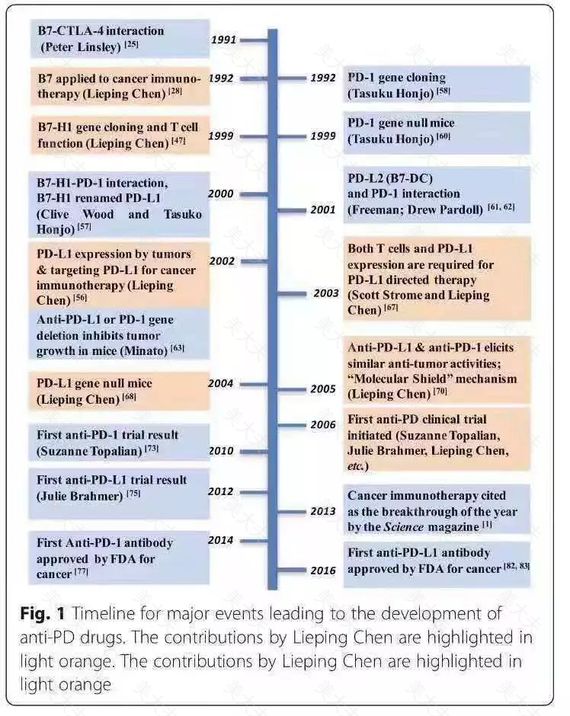
【图片来自于文献: PD-1, PD-L1 (B7-H1) and Tumor-Site Immune Modulation Therapy: The Historical Perspective】
此次诺奖遗漏了陈列平教授,有很多科研同行通过社交媒体表达了对此的失望,或者不满,认为本次诺奖有失公允,各种揣测纷至沓来。虽然现场有记者询问为何陈教授未获奖,诺奖评委会回答:“有些科学家获奖了,有些没有获奖,我们只能评论那些获奖者,无法对未获奖的科学家进行评论。科学的发现的确是很多科学家研究的结果。”
在首届全球华人科学家创新转化30人高峰论坛上,科学家、企业家、投资家一起,探讨了“如何提高华人科学家在全球的影响力和话语权”这一议题,大家认为,华人科学家不仅需要进行一以贯之的原创研究,更需要具备“研究以外”的能力。不仅需要勇于发声,更要学会如何发声,具备“讲故事”的传播能力。善于使用策略,发挥影响力,并加强团队合作,达到“众人拾柴火焰高”的目的。“我们中国人不擅于讲故事、将其变成简单得额概念让大家接受,没有简练地表达自己,这个可能是我们最大的缺陷。“把复杂的原理提炼成简单的概念、易懂的故事,华人在这一方面是有欠缺。” 陈列平教授在论坛上如是说。“It proves that promotion of work is more important than the work itself....”陈列平教授今天评论道。
原因可能有很多,华人的不善言辞,不善自我营销,以及地位等等。
好在,此次诺奖的颁布是对整个肿瘤免疫治疗领域的承认,这个领域能为更多的病人带来期望,除了放化疗之外,也许,他们能够使用自己的内在力量—“免疫”,抗击癌症。无论是CTLA-4,还是PD-1/PD-L1,这只是肿瘤免疫疗法的开端,正如陈列平教授在获得2018“Giants of Cancer Care”后接受记者采访时所言:“我期待更多的发现和进展浮出水面,这个领域比以往任何时候都更加充满希望。”继续寻找新的靶点、新的机制,延长患者的生命时间,提高生活质量,继续享受天伦,延续更多病人“活下去”的希望,远比勋章加身更为重要。
本文由董增军总裁、茅幸博士整理编写,部分内容引用自微信公号“CST博士互助平台”。